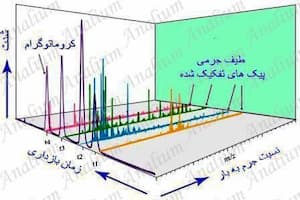
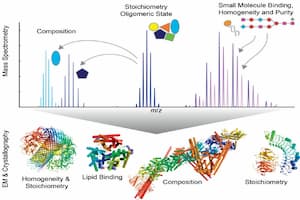
منابع یونش طیف سنجی جرمی نقش بسیار مهمی در آنالیز دارند. به همین علت تا کنون منابع یونش متنوعی توسعه داده شده اند. در ادامه انواع روش های یونش که در طیف سنجی جرمی شناخته شده اند را شرح می دهیم.
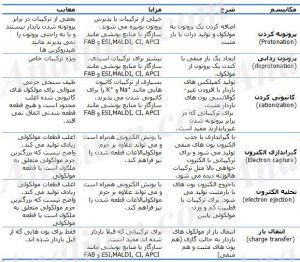
روش های یونش به مکانیسم های متفاوتی اتلاق می شود که برای یونی کردن ترکیبات در نمونه به کار می رود. این مکانیسم ها شامل پروتونه کردن (Protonation)، پروتون زدایی (deprotonation)، کاتیونی کردن (cationization)، انتقال بار (charge transfer)، تخلیه الکترون (electron ejection) و گیراندازی الکترون (Electron capture) هستند. جدول 2 انواع مکانیسم یونش در طیف سنجی جرمی به همراه معایب و مزایای هر کدام هر مکانیسم را نشان می دهد.
منابع یونش (ionization source) به دو دسته گازی و واجذبی تقسیم می شوند: در نوع گازی ابتدا مولکول های نمونه به حالت گازی در آمده و سپس به یون تبدیل می شوند و در نوع واجذبی مستقیما از حالت مایع یا جامد به یون های گاز تبدیل می شوند.
منابع یونش از نظر میزان یونش نیز به دو دسته یونش سخت (hard ionization) و یونش نرم (ionization soft) تقسیم می شوند. در یونش سخت انرژی زیادی به مولکول داده می شود تا به حالت برانگیخته در آید بنابراین در برگشت به حالت پایه متحمل شکست های فراوان شده و تعداد قطعات یونی که ایجاد می شود، زیاد است. در یونش نرم انرژی زیادی به مولکول داده نمی شود در نتیجه تعداد یون های حاصل شده خیلی کم است و در بعضی مواقع فقط در حد تولید یون مولکول است. یون مولکول (Molecular Ion)، مولکول یونیزه و سالمی ست که فقط یک الکترون از آن برداشته شده است بنابراین جرم مولکولی برابر با مولکول اولیه دارد و تفاوت ساختاری نیز با آن ندارد.
جدول 2- انواع مکانیسم یونش در طیف سنجی جرمی به همراه معایب و مزایای هر کدام
تا سال 1980 تنها منبع یونش یونش الکترونی (EI) بود که فقط محدود به مولکول های کوچک بود و برای بیومولکول ها کارایی نداشت. اما ابداع تکنیک های بمباران سریع اتمی (FAB) ، واجذب-یونش لیزری به کمک ماتریس (MALDI) و.. انقلابی در آنالیز بیومولکول ها به وجود آورد. در ادامه چند منبع یونش پرکاربرد را شرح خواهیم داد.
یونش الکترونی (EI)
یونش الکترونی (electron ionization) از مهم ترین منابع یونش برای آنالیزهای معمول (routine) مولکول های کوچک، آب گریز و از نظر حرارتی پایدار است و به طور گسترده ای در طیف سنج های جرمی استفاده می شود. به دلیل یونش سخت در این روش قطعات یونی زیادی تولید می شود. البته، با وجود پایگاه داده (database) یا کتابخانه های جرمی بسیار قوی از طیف های جرمی ترکیبات، قطعه قطعه شدن یونی در بدست آوردن اطلاعات ساختاری می تواند بسیار مفید واقع شود.
این منبع یونش طراحی ساده ای دارد. نمونه گازی با گذر از یک لوله مویی (capillary) یا نمونه های روی یک پروب با واجذبی حرارتی، توسط پرتوی از الکترون های پرانرژی (70eV) بمباران می شود. این روش مناسب کوپل شدن با کروماتوگرافی گازی-طیف سنج جرمی (GC/MS) است. کارایی این روش برای ترکیبات با وزن مولکولی بالای 400 Da دالتون کم است چون مولکول های بزرگ و ناپایدار حرارتی، قبل از تبخیر در اثر حرارت تجزیه می شوند. از مشکلات اصلی واجذبی حرارتی نمونه ها در یونش الکترونی، غیرفرار بودن مولکول های بزرگ، تجزیه حرارتی، قطعه قطعه شدن زیاد مولکول ها و احتمال کم تولید یون مولکول است.
یونش شیمیایی (CI)
در روش یونش شیمیایی (Chemical Ionization) یک پرتو الکترونی یک معرف گازی مانند متان، ایزوبوتان یا آمونیاک را یونیزه می کند. در اثر این یونش، یون هایی مانندCH5+ و NH4+ تولید می شوند که انرژی کمتری از پرتو الکترونی داشته و یونش ملایم تری اتفاق می افتد. بنابراین برخلاف روش یونش الکترونی در این روش احتمال تشکیل یون مولکول بالاست و قطعه قطعه شدن کمتری نیز صورت می گیرد. اما مشابه EI باید نمونه های از نظز حرارتی پایدار باشند تا حین حرارت دادن و تبخیر کردن تجزیه نشوند.
یونش شیمیایی منفی (negative chemical ionization, NCI) با گیراندازی الکترون برای نمونه هایی انجام می شود که یک گروه الکترون گیرنده مانند فلور یا نیتروبنزن در ساختار مولکولی خود دارند. روش NCI حساسیت و گزینش پذیری بسیار بالاتری از EI و CI دارد. اگرچه تعداد ترکیبات کمی دارنده گروه های الکترون گیرنده هستند تا بتوان از روش NCI استفاده کرد اما می توان با مشتق سازی یک گروه الکترون گیرنده به مولکول اضافه کرد تا سبب افزایش حساسیت و گزینش پذیری آنالیز ترکیب مورد نظر گردد.
یونش الکترواسپری (ESI)
در روش یونش الکترواسپری (Electrospray Ionization, ESI) ، نمونه در یک حلال قطبی و فرار حل شده و سپس از یک لوله مویی از جنس استیل یا سیلیکون با سرعت جریان حدود 1میلی لیتر بر دقیقه پمپ شده و عبور داده می شود. یک ولتاژ بالا (Vه5000-700) بین نوک لوله مویی و یک الکترود کمکی (counter electrode) اعمال می شود. این میدان الکتریکی قوی سبب می شود که نمونه که از نوک لوله مویینه خارج می شود به صورت آئروسلی (Aerosol) از قطرات باردار باشند.
از گاز نیتروژن برای اسپری کردن و راندن این قطرات به سمت طیف سنج استفاده می شود. ضمن اینکه جریان گرم نیتروژن باعث تبخیر حلال از قطره ها، کاهش اندازه قطرات و افزایش چگالی بار روی آنها می شود. در نهایت، یون های باردار نمونه بدون حلال با عبور از یک مخروط وارد منطقه خلاء و سپس از طریق یک دیافراگم وارد طیف سنج با خلاء بالا می شوند. شکل 1 شمای کلی منبع یونش ESI را نشان می دهد.
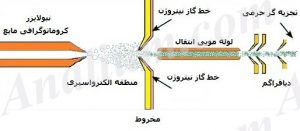
ESI به دلیل ورود مداوم نمونه مناسب روش های HPLC و الکتروفورز است. این روش به طور معمول برای پپتیدها، پروتئین ها، کربوهیدرات ها، پلیمر های سنتزی و لیپید ها مورد استفاده قرار می گیرد. از مزایای این روش یونش نرم (soft ionization) ترکیبات، حساسیت کم و در حد فمتومول ( 15-110مول)، محدوده جرم مولکولی تا 7000 دالتون، سازگاری با کروماتوگرافی مایع، اثرات ماتریسی کم و قابلیت استفاده در طیف سنج های جرمی متوالی (tandom mass spectrometer) است اما حضور نمک، معرف های زوج-یون (ion-pair) و ماتریس های پیچیده سبب کاهش حساسیت می شوند و در آنالیز همزمان مخلوط ها کارایی لازم را ندارد.
یونش شیمیایی تحت فشار اتمسفری (APCI)
یونش شیمیایی تحت فشار اتمسفری (Atmospheric pressure chemical ionization, APCI) یک منبع یونش مهم است زیرا یون ها مستقیما از محلول تولید شده و توانایی آنالیز ترکیبات نسبتا غیرقطبی را نیز داراست. مشابه روش یونش الکترواسپری، جریان مایع مستقیما وارد منبع یونش می شود. ولی در اینجا قطرات باردار نشده و با حرارت حلال زدایی و تبخیر می شوند. نمونه بخار شده از یک منطقه واکنش یون-مولکول در فشار اتمسفری عبور می کند. مولکول های حلال با تخلیه الکتریکی یونیزه می شوند.
چون مولکول های آنالیت در فشار اتمسفری تمایل به تجمع با مولکول های حلال دارند بنابراین کارایی یونش مولکول های آنالیت توسط مولکول های حلال بسیار بالاست. با انتقال پروتون یا کندن پروتون توانایی تولید هم یون های مثبت و هم منفی را دارد. به خاطر وجود حلال یونش ملایم بوده و قطعه قطعه شدن زیاد اتفاق نمی افتد.
واجذب-یونش لیزری به کمک ماتریس (MALDI)
در روش واجذب-یونش لیزری به کمک ماتریس (Matrix-assisted laser desorption/ionization, MALDI) ، آنالیت در ماتریسی از یک ترکیب غالبا جاذب UV کریستالیزه شده و پخش می گردد. این ماتریس روی یک سطح فلزی قرار گرفته و سپس به محفظه خلا وارد می شود. تاباندن یک پرتو لیزری و متمرکز کردن آن بر روی نمونه، سبب واجذبی و یونیزاسیون آنالیت و ماتریس می شود.
ماتریس یک ماده جامد غیر فرار است که جاذب پرتو لیزر بوده و هم چنین مولکول های آنالیت را از تخریب شدن با پرتو لیزری حفظ می کند. پرتو دهی این مخلوط با لیزر و جذب پرتو لیزری توسط ماتریس، سبب تبخیر و یونیزه شدن ماتریس و آنالیت خواهد شد. حساسیت خوب، محدوده جرمی تا 300000 دالتون، یونش ملایم بدون قطعه قطعه شدن زیاد آنالیت، عدم مزاحمت غلظت بالای نمک و توانایی آنالیز مخلوط های پیچیده از مزایای این روش است که سبب شده تا کاربرد گسترده ای در آنالیز بیومولکول ها داشته باشند. از مشکلات این روش یافتن یک ماتریس مناسب و احتمال تخریب فوتونی آنالیت است. روش آماده سازی ماتریس تاثیر زیادی بر کیفیت طیف جرمی خواهد داشت.
بمباران سریع اتمی (FAB)
بمباران سریع اتمی (Fast Atom Bombardment) مشابه روش MALDI از یک ماتریس و پرتو باانرژی بالا برای واجذبی و تولید یون استفاده می کند. پرتوی از اتم های خنثی زنون یا اتم های سزیوم (Cs+) برای بیرون انداختن نمونه و ماتریس، از پروبی که مستقیما وارد منبع یونش شده، استفاده می شود. ماتریس FAB یک مایع غیرفرار مانند گلیسرول، تیوگلیسرول، دی اتانول آمین و .. است که برای تسهیل واجذبی و یونش نمونه بکار می رود و با جذب بیشتر انرژی تجزیه و تخریب شدن نمونه را به حداقل می رساند.
توجه شود که در روش MALDI از لیزر پالسی ولی در FAB از یونی پیوسته استفاده می شود و در MALDI ماتریس یک جامد کریستالی ست ولی در FAB ماتریس یک مایع غیر فرار است. روش 1000i FAB بار حساسیت کمتری نسبت به MALDI دارد.
انتخاب منبع یونش
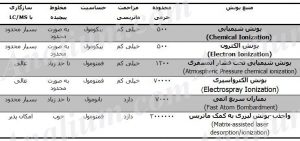
انتخاب منبع یونش به نوع نمونه و طیف سنج جرمی بستگی دارد. اگرچه پارامترهای دیگر (جدول 1) نیز از اهمیت بالایی برخوردارند. جدول 2 منابع یونش مختلف را از نظر پارامترهای مانند محدوده جرمی، مزاحمت ماتریسی، حساسیت، توانایی آنالیز مخلوط های پیچیده و سازگاری برای جفت شدن با کروماتوگرافی مایع-طیف سنج جرمی (LC/MS) را برای مقایسه بیشتر فهرست کرده است.
جدول 2 مقایسه کلی منابع یونش در طیف سنجی جرمی
توجه شود منابع یونشی فوق برای یونش مولکول ها و و استفاده در طیف سنجی جرمی مولکولی ست. در طیف سنجی جرمی اتمی که به آن طیف سنجی معدنی (inorganic mass spectrometry) نیز گفته می شود، از اتمی کننده پلاسما که نقش یون ساز را نیز دارند، به عنوان منبع یونش استفاده می شود و طیف سنج جرمی برای جداسازی یون های استفاده می شود.