کروماتوگرافی (Chromatography) متداول ترین روش جداسازی ست که با پیشرفت های دستگاهی به روشی ارزشمند برای جدا سازی، اندازه گیری و شناسائی مواد تبدیل شده است.
کروماتوگرافی کاربرد وسیعی در بسیاری از زمینه ها شامل شیمی، داروسازی، پتروشیمی، مواد غذایی، زیست فناوری و غیره پیدا کرده است. روش های کروماتوگرافی برای جداسازی مخلوط ترکیبات، شناسایی ترکیبات ناشناخته یا مجهول، تخمین خلوص و غلظت مواد، نظارت در تولید دارو در صنایع داروسازی و بیوتکنولوژی، در پزشکی قانونی برای آنالیز نمونه های بیولوژیک، رنگ، مواد منفجره و .. کاربرد بسیار زیادی دارند. اهمیت این دسته از روش ها وقتی مشخص می شود که بدانیم از سال 1937 تا 1972 دوازده جایزه نوبل به تحقیقاتی تعلق گرفت که روش های کروماتوگرافی نقش حیاتی در انجام آنها داشت.
این روش اولین بار توسط یک دانشمند روسی به نام Tswett، برای جداسازی رنگ های گیاهی با عبور دادن محلولی حاوی این ترکیبات از ستونی پر شده با کربنات کلسیم، به کار برده شد. این ترکیبات به صورت باندهای رنگی در انتهای ستون جدا شدند. کلمه chroma به زبان یونانی یعنی رنگ و graphein به معنای نوشتن است.
اصول و مبانی کروماتوگرافی
اساس کروماتوگرافی پخش انتخابی اجزاء یک نمونه بین دو فاز مختلف است. در واقع تفاوت سرعت اجزاء مختلف در عبور از یک سیستم متشکل از دو فاز مبنای جداسازی در روش های کروماتوگرافی ست. یکی از این فازها که سطح زیادی دارد را فاز ساکن (Stationary Phase) و فاز دیگر را فاز متحرك (Mobile Phase) گویند. شکل 1 مراحل مختلف جداسازی اجزاء یک نمونه در روش های کروماتوگرافی را به تصویر کشیده است.
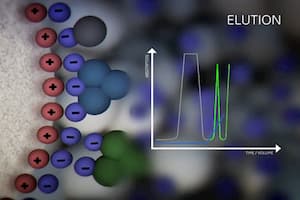
وقتی فاز متحرک که حاوی نمونه مورد نظر است از ستون عبور داده می شود، در تماس با فاز ساکن، نمونه بین فازمتحرک و ساکن تقسیم می شود. این تعادل و انتقال بین دوفاز در طی ستون دائما صورت می گیرد و منجر به یک سرعت متوسط برای هر جزء می شود. در نتیجه این سرعت های مهاجرت متفاوت، اجزاء نمونه به صورت باند از هم جدا می شوند که در نتیجه می توان به صورت کیفی و کمی آنالیز شوند. این باندهای مجزا در زمان های متفاوتی از ستون بیرون می آیند. اجزایی که در فاز ساکن بیشتر نگه داشته می شوند، کندتر حرکت کرده و دیرتر به انتهای ستون می رسند.
اجزایی که توسط فاز ساکن کمتر نگه داشته می شوند، زودتر از ستون خارج می شوند (شکل 1-الف). اگر در انتهای ستون یک آشکارساز قرار گیرد پاسخ آشکارساز برحسب زمان یک کروماتوگرام (chromatogram) است که از چند پیک تشکیل شده است (شکل 1-ب). کروماتوگرام اطلاعات کیفی و کمی مفیدی از آنالیز مربوطه را فراهم می کند.

در تمامی روش های کروماتوگرافی جداسازی بر پایه تفاوت مقدار ماده موردنظر در دو فاز ساکن و فاز متحرک انجام می شود. هر آنالیتی در تعادل بین دو فاز است:
Amobile↔Astationary
این رابطه تعادلی با پارامتری به نام ضریب تقسیم (partition coefficient) (K) بیان می کنند.
(1) K=Cs/Cm
در رابطه (1) Cs غلظت آنالیت در فاز ساکن و Cm غلظت آنالیت در فاز متحرک است.
زمان بین تزریق نمونه و رسیدن آنالیت به آشکارساز در انتهای ستون را زمان بازداری (retention time) گویند. هر آنالیت در نمونه زمان بازداری متفاوتی دارد. زمان مرده (tM) زمان موردنیاز برای رسیدن گونه بازداری نشده به آشکارساز است که در واقع نشانگر سرعت متوسط فاز متحرک نیز هست.
ضریب بازداری یک پارامتر بسیار مهم است که برای توصیف سرعت مهاجرت آنالیت ها در ستون ها به کار برده می شود. برای گونه A، ضریب بازداری (k’A) به صورت زیر تعریف می شود:
k’A=KA.Vs/Vm=(tR-tM)/tM (2)
در رابطه فوق، KA ثابت توزیع برای گونه A ، Vs و Vm به ترتیب حجم فاز ساکن و حجم فاز متحرک و tR و tM نیز به ترتیب زمان بازداری گونه A و زمان مرده ستون را نشان می دهند.
تئوری بشقابک های فرضی
برای تخمین کارایی ستون از تئوری بشقابک های فرضی (Plates) استفاده می شود. این تئوری با تشبیه ستون های کروماتوگرافی به ستون های تقطیر، فرض را بر این قرار می دهد که هر ستون از تعدادی لایه های باریک و کاملا مجزا از هم تشکیل شده است. به هر یک از این لایه ها، بشقابک های فرضی گفته می شود. در هرکدام از این بشقابک ها، آنالیت در تعادلی بین فاز متحرک و ساکن قرار دارد و در نهایت با انتقال بین بشقابکها عمل جداسازی صورت می پذیرد.
کارایی هر ستون به تعداد بشقابکهای موجود در ستون و یا به عبارت دیگر به تعداد تعادل های ایجاد شده در ستون بستگی دارد. تعداد بشقابک های فرضی به ارتفاع هر بشقابک (plate height, H) و طول ستون (L) مرتبط است و از رابطه ساده زیر محاسبه می شود:
N=L/H (3)
هرچه تعداد بشقابک های فرضی (N) بیشتر باشد، کارایی ستون نیز بالاتر خواهد بود. با توجه به شکل گوسی پیک ها و روابط بین پهنای پیک و حجم بازداری، رابطه زیر برای کارایی به دست می آید که نشان می دهد هر ستونی برای هر آنالیتی کارایی متفاوتی دارد، چون زمان بازداری متفاوتی دارند:
در این رابطه w1/2 پهنای پیک در نصف ارتفاع است.
N=(5.55tR2)/(W1/2)2 (4)
ضریب گزینش پذیری (selectivity factor) برای یک ستون برای جداسازی دو گونه A و B به صورت زیر تعریف می شود:
α=KA/KB=k’A/k’B=(tR)B-tM/(tR)A-tM (5)
KA و KB ثابت توزیع گونه A و B هستند و α ضریب گزینش پذیری ست. در این رابطه گونه ای که بیشتر بازداری می شود، در صورت قر ار می گیرد و بنابراین α همیشه بزرگتر از یک است. α برابر با یک یعنی ستون انتخاب شده هیچ گزینشی بین دو گونه A و B ندارد و این دو با هم بیرون می آیند.
در ضریب گزینش پذیری جداسازی مرکز پیک یا باندها از در نظر گرفته می شود و عرض پیک یا پهن شدگی آن را لحاظ نمی شود. تفکیک (Resolution) معیار بهتری برای جداسازی دو پیک است که به صورت زیر تعریف می شود:
R=(2[(tR)B-(tR)A]/(WA+WB) (6)
WA و WB به ترتیب عرض پیک گونه های A و B هستند. هم چنین تفکیک با رابطه زیر به کارایی ستون و ضریب گرینش پذیری مرتبط می شود:
R=(N0.5/4)[(α-1)/α][((1+k’B)/k’B] (7)
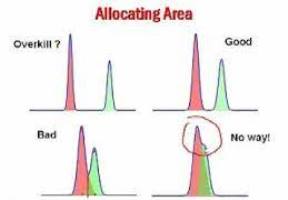
بر اساس رابطه (7) قدرت تفکیک یک ستون به کارایی ستون، ضریب گزینش پذیری و فاکتور بازداری بستگی دارد. برای بدست آوردن بالاترین مقدار R سه ترم معادله (7) باید افزایش یابند. تعداد بشقابک ها که با افزایش طول ستون و افزایش زمان بازداری و در نتیجه پهن شدگی پیک همراه خواهد بود. اما کاهش قطر ذرات فاز ساکن سبب کاهش ارتفاع بشقابک و افزایش کارایی ستون خواهد شد.
فاکتور بازداری با تغییر ترکیب حلال در کروماتوگرافی مایع و با تغییر دما در کروماتوگرافی گازی قابل کنترل است. مقدار R=1 یعنی جداسازی صورت گرفته است و برای مقاصد آنالیزی کفایت می کند و R≥1.5 یعنی جداسازی کامل صورت گرفته است.
تئوری سرعت
برخلاف تئوری بشقابک، تئوری سرعت (rate theory) شرح واقعی تری از فرایندهای داخل ستون ارائه می دهد. در تئوری بشقابک تعادل بی نهایت سریع در نظر گرفته می شود اما در تئوری سرعت زمانی طول می کشد تا حل شونده بین فاز متحرک و ساکن به تعادل برسد. بنابراین شکل پیک کروماتوگرافی به سرعت شویش حل شونده بستگی دارد. به کمک مکانیسم های مختلفی که برای پهن شدگی پیک ها در نظر گرفته می شود، ارتفاع بشقابک (H) با معادله ون دیمتر (Van Deemter) به صورت زیر به دست می آید:
H=A+B/u+Cu (8)
در این رابطه u سرعت متوسط فاز متحرک و A,B و C ثوابت هستند.
A نفوذ ادی (Eddy diffusion): وقتی فاز متحرک از ستونی که با فاز ساکن پرشده عبور می کند، مولکول های حل شونده مسیرهای مختلف تصادفی در فاز ساکن خواهند داشت. این مسرهای مختلف طول مسیر متفاوتی خواهند داشت و در نتیجه سبب پهن شدگی باند حل شونده می شوند.
B نفوذ طولی (longitudinal diffusion): غلظت آنالیت در لبه های کمتر از مرکز باند است و مولکول ها از مرکز به سمت کناره ها انتشار می یابند. که این پدیده نیز سبب پهن شدگی پیک می گردد. اگر سرعت فاز متحرک آنقدر بالا باشد که آنالیت زمان کمی را در ستون صرف کند اثرات این نوع نفوذ کاسته شده و پهن شدگی کمتر می شود.
C مقاومت در برابر انتقال جرم (resistance to mass transfer): یک زمان مشخصی طول می کشد تا آنالیت بین فاز متحرک و ثابت به تعادل برسد. اگر سرعت فاز متحرک بالا باشد، و آنالیت میل ترکیبی قوی با فاز ساکن داشته باشد، در نتیجه آنالیت در فاز متحرک پیش از آنالیت در فاز ساکن حرکت خواهد کرد و باند آنالیت پهن تر خواهد شد. هرچه سرعت فاز متحرک بالاتر باشد پهن شدگی بیشتر خواهد بود.
دستگاهوری کلی برای تمام این روش ها کروماتوگرافی شامل قسمت تزریق (injection)، ستون و آشکار ساز است.
انواع روش کروماتوگرافی
کروماتوگرافی با توجه به طبيعت فازهای ساکن و متحرک به دستههای مختلفی تقسيم میشود. روش های جداسازی که براساس پخش ماده مورد تجزیه بین یک فاز متحرک مایع و یک فاز ساکن مایع یا جامد قرار دارند، تحت نام کروماتوگرافی مایع (liquid chromatography) دسته بندی می شوند. در کروماتوگرافی گازی (gas chromatography) فاز متحرک یک گاز است که آن را گاز حامل (carrier gas) می نامند. فاز متحرک از روی فاز ساکن که امتزاج ناپذیر (immiscible) است و به شکل ستون یا در یک سطح ثابت شده است، عبور داده می شود. یک تقسیم بندی دیگر نیز بر اساس نوع تعادلی ست که برای انتقال حل شونده ها (solute) بین دو فاز صورت می گیرد. این تعادل ها عبارتند از تقسیم (partition) بین دو فاز، جذب سطحی (Adsorption) و تعویض یونی (Ion exchange).
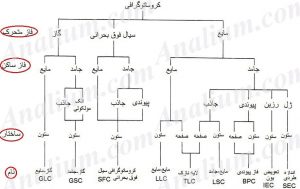
تقسیم بندی انواع روش های کروماتوگرافی با توجه به نوع فاز متحرک، فاز ساکن و شکل استفاده از فاز ساکن در شکل 2 ترسیم شده است. در کروماتوگرافی ستونی فاز ساکن در ستون های باریک نگه داشته می شود و فاز متحرک با فشار از روی آن عبور داده می شود. در کروماتوگرافی مسطح (planar) فاز ساکن بر روی یک صفحه مسطح یا لابلای کاغذ اندوده شده و فاز متحرک تحت تاثیر جاذبه یا خاصیت مویینگی از روی فاز ساکن عبور داده می شود.
آنالیز کیفی و کمی
از آنجایی که زمان بازداری برای هر ماده در یک سیستم و شرایط خاص آزمایشگاهی ثابت و مشخص می باشد، می توان از آن جهت تعیین نوع آنالیت استفاده کرد. به این منظور کروماتوگرام آنالیت را با کروماتوگرام به دست آمده از استاندارد آن آنالیت مقایسه می کنند. در صورت یکسان بودن زمان بازداری می توان با قطعیت نوع ماده را تعیین کرد.
آنالیز کمی
آنالیز کمی تعیین مقدار مطلق یا فراوانی نسبی، که معمولا با غلظت مشخص می شود است، یک یا چند جزء در نمونه موردنظر است.
استاندارد خارجی (External standard): روش استاندارد خارجی متداول ترین روش در اندازه گیری های کمی ست. در این روش یک یا چند استاندارد با غلظت مشخص از آنالیت مورد نظر تحت شرایط دستگاهی و آزمایشگاهی مشابه نمونه ها آنالیز می شود. منحنی کالیبراسیون حاصل از ارتفاع یا سطح زیر پیک کروماتوگرام محلول های استاندارد بر حسب غلظت آنالیت ها در محلول های استاندارد رسم می شود. با استفاده از معادله خط بدست آمده و با اندازه گیری ارتفاع یا سطح زیر پیک نمونه مجهول مقدار دقیق آنالیت محاسبه می شود.
افزایش استاندارد (standard addition): در این روش تطابق ماتریس نمونه و استانداردها صورت می گیرد. بنابراین این روش مواقعی بکار می رود که اثر ماتریس در نتایج کمی زیاد است و امکان حذف ماتریس وجود ندارد.
استاندارد داخلی (Internal standard): استاندارد داخلی ماده ای با ساختار مولکولی مشابه آنالیت است که پیکی جدا از آنالیت و نزدیک پیک آنالیت دارد. در این روش مقادیر مشخصی از یک استاندارد داخلی به استانداردها و نمونه ها اضافه می شود. این روش برای حذف خطاهای آزمایش و ناپایداری دستگاه به کار می رود.
برای اطلاعات بیشتر به بخش کالیبراسیون و رگرسیون مراجعه کنید.



12 Comments
نظرات بسته شده است.